针对HER2的靶向药物
与 EGFR 靶向治疗类似,靶向 HER2 的药物可分为单克隆抗体和激酶抑制剂(详见下表):
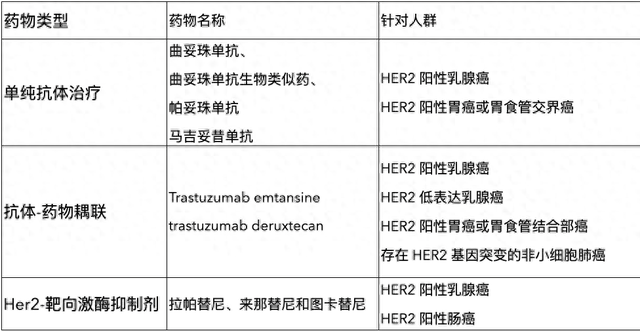
从细胞外阻断 HER2 的单克隆抗体
从细胞外阻断 HER2 并递送化疗药物的抗体偶联药物
从细胞内阻断 HER2 激酶结构域的激酶抑制剂
靶向 HER2 的单克隆抗体
目前有五种靶向 HER2 的抗体被批准用于癌症治疗:曲妥珠单抗、帕妥珠单抗、马吉妥昔单抗、恩美曲妥珠单抗(T-DM1)和德曲妥珠单抗(T-DXd)。其中前三种为 “裸” 抗体,即抗体结构未进行任何修饰;另外两种是将化疗药物递送至靶细胞的抗体偶联药物(ADC)。
1.1 作用机制
曲妥珠单抗是首个获批的 HER2 靶向抗体,其作用机制包括:
阻止 HER2 同源二聚体(HER2:HER2)激活信号通路,对 HER2:HER3 或 HER2:EGFR 异源二聚体作用较弱。
招募巨噬细胞和自然杀伤细胞等免疫细胞,杀伤 HER2 阳性癌细胞。
防止 HER2 胞外段脱落 —— 若 HER2 蛋白断裂,残留于细胞膜的 p95 片段活性极强。
可能抑制 HER2 同源或异源二聚化。
诱导 HER2 降解。
相比之下,帕妥珠单抗的主要作用是阻止HER2与EGFR或HER3结合 。二者作用机制互补,部分临床试验显示联合使用效果更佳。
恩美曲妥珠单抗(T-DM1)和德曲妥珠单抗(T-DXd)则属于 ADC 类药物,由曲妥珠单抗与强效化疗药物(恩美坦辛或德鲁替康)偶联而成。曲妥珠单抗及其他 HER2 靶向抗体的作用机制总结见图1。
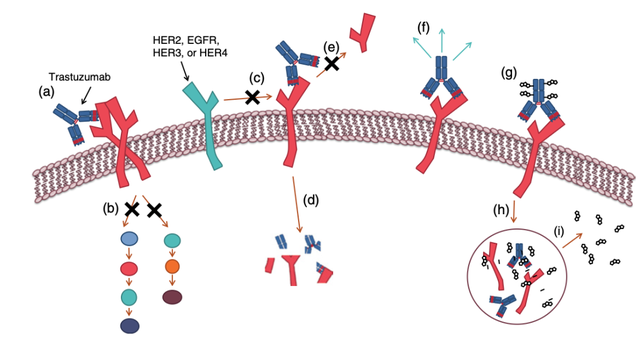
图1 HER2 靶向抗体的作用机制。(a) 曲妥珠单抗附着在细胞膜附近的 HER2 上。(b) 它可防止 HER2 同源二聚体和异源二聚体激活信号通路。(c) 帕妥珠单抗(在一定程度上还有曲妥珠单抗)可阻止 HER2 与 HER2、EGFR 或 HER3 配对,从而防止信号通路激活(未配对的生长因子受体无法激活信号通路)。(d) 曲妥珠单抗触发 HER2 的破坏,并且 (e) 防止 HER2 从细胞表面断裂和脱落。(f) 曲妥珠单抗和帕妥珠单抗均可激活白细胞。马吉妥昔单抗在这方面的设计更为出色。(g) 抗体药物偶联物(ADCs),如恩美曲妥珠单抗(T-DM1)和德曲妥珠单抗(T-Dx),具备曲妥珠单抗的所有功能,而且还连接了化疗药物。(h) 一旦进入细胞内,T-DM1 和 T-Dx 就会分解。(i) 化疗药物渗入细胞内。
1.2 适用人群
HER2 靶向治疗主要用于 HER2 阳性乳腺癌或胃癌患者——这类患者的癌细胞表面HER2蛋白水平极高和/或HER2基因存在扩增(图 2)。但 “HER2 阳性” 的具体定义取决于癌症检测方法和类型。例如,若未进行基因分析,医生无法确定 HER2 基因是否扩增,此时 “HER2 阳性” 仅指通过免疫组化(IHC)检测的细胞表面 HER2 蛋白表达量。
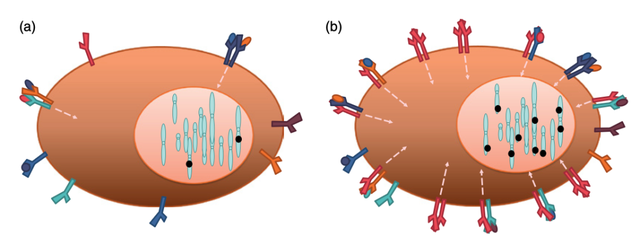
图2 HER2 阳性癌症的 HER2 基因有额外拷贝,并且(或)其细胞表面有过量的 HER2 蛋白。(a) 正常细胞有两个 HER2 基因拷贝(位于 17 号染色体上),产生的 HER2 蛋白极少。细胞表面的配对受体仅提供维持细胞存活所需的足够信号通路激活量。(b) HER2 基因扩增导致 HER2 蛋白过度生成,HER2 蛋白会自身配对,并与其他 HER 家族成员(即 EGFR、HER3 和 HER4)配对。这会增强信号通路的活性,促使细胞增殖和存活。黑点表示 HER2 基因每个拷贝的位置。
曲妥珠单抗于 2000 年在欧洲首次获批用于治疗 HER2 阳性乳腺癌,2010 年适应症扩展至 HER2 阳性胃癌。帕妥珠单抗、T-DM1、T-DXd 和马吉妥昔单抗以及部分激酶抑制剂也被批准用于乳腺癌治疗。
HER2 阳性乳腺癌侵袭性强,治疗后易转移复发。但HER2靶向治疗已逆转了其与不良预后的关联。约15%-20% 的乳腺癌和胃癌为HER2阳性,但两类癌症中 “HER2阳性” 的定义存在差异:胃癌细胞表面HER2表达异质性高,且免疫组化(蛋白检测)与原位杂交(基因扩增检测)结果常不一致 。科学家认为,这种高度异质性是 HER2 靶向治疗在胃癌中疗效不如乳腺癌的原因。
1.3 HER2 靶向治疗的进展
与恩美曲妥珠单抗(T-DM1)相比,德曲妥珠单抗(T-DXd)有多项改进:例如,每个抗体偶联的药物分子更多,且药物与抗体的连接子在癌细胞内更易断裂。这使T-DXd 在T-DM1失败的情况下仍可能有效。2022 年,基于DESTINY-Breast04 研究结果,欧美监管机构批准T-DXd用于治疗 HER2 低表达乳腺癌。约50% 的乳腺癌为HER2低表达(远高于传统 HER2阳性比例)。
HER2低表达癌症是指细胞表面有一定HER2但未达阳性标准,且HER2基因无扩增的肿瘤,包括约50%的激素受体阳性乳腺癌和30%的三阴性乳腺癌。T-DXd等药物偶联物的出现,也为治疗除乳腺癌和胃癌外的HER2阳性及HER2低表达癌症创造了新机会。非小细胞肺癌、唾液腺癌、肠癌、胆道癌、子宫癌、卵巢癌和胰腺癌等多种癌症中,部分患者的癌细胞表面存在一定HER2和/或 HER2过度激活。
过去,曲妥珠单抗、拉帕替尼等HER2靶向治疗对这些患者获益有限。但尤其是T-DXd的问世,使HER2靶向治疗的临床试验结果不断改善。2022年,FDA 加速批准德曲妥珠单抗用于治疗携带 HER2 突变的非小细胞肺癌患者。
1.4 耐药原因
尽管 HER2 靶向抗体已被证实非常有效(尤其针对HER2阳性乳腺癌),但并非对所有患者都有效,且对转移性癌症患者的获益通常是暂时的(尽管可能持续数月甚至数年)。
关于 HER2 靶向抗体耐药机制的认知多来自对曲妥珠单抗耐药乳腺癌的研究,已发现的耐药机制包括(图3):
脑等受保护部位的癌细胞逃避治疗。
激活 PI3K/AKT/mTOR 通路的突变使 HER2 功能冗余,阻断 HER2 无效。
HER2 结构改变:癌细胞可能产生缺乏曲妥珠单抗结合位点的短链 HER2(p95),或 HER2 激酶结构域过度激活。
曲妥珠单抗吸引和激活免疫细胞的能力对疗效至关重要:肿瘤浸润免疫细胞少或免疫抑制蛋白水平高的患者,可能对曲妥珠单抗反应不佳。
若癌细胞表面存在 EGFR、HER3、MET、IGF-1 或 EphA2 等其他生长因子受体,即使 HER2 被阻断,这些受体仍可激活信号通路。
若 EGFR 或 HER3 与 HER2 形成二聚体,曲妥珠单抗无法完全阻断(帕妥珠单抗或拉帕替尼等激酶抑制剂可预防或阻断此类二聚体)。
若癌细胞含大量雌激素受体(ER),会诱导多种生长因子受体表达并激活信号通路,抵消曲妥珠单抗的作用。
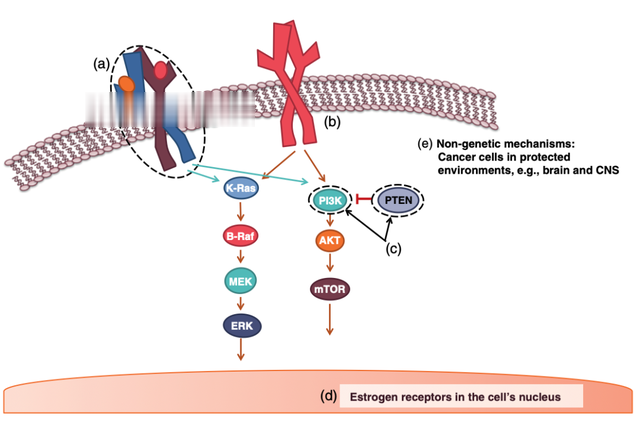
图3 乳腺癌细胞对 HER2 靶向抗体产生耐药性的一些原因。
(a)一些对曲妥珠单抗耐药的细胞发生了影响 HER2 基因的突变。因此,它们产生过度活跃的 HER2,或者产生一种缺少曲妥珠单抗结合位点的 HER2 变体。
(b)另一个耐药原因是细胞表面存在其他生长因子受体。
(c)影响 PI3K 通路的突变,例如 PIK3CA 基因的突变导致 PI3K 过度活跃,或 PTEN 缺失。
(d)如果细胞核中有大量活跃的雌激素受体,这些受体可以保护细胞免于死亡。
(e)处于受保护环境(如大脑)中的癌细胞,很大程度上难以受到像曲妥珠单抗这样难以穿过血脑屏障的抗体治疗的影响。
基于上述认知,多项临床试验探索了联合治疗方案,例如曲妥珠单抗联合帕妥珠单抗或拉帕替尼,或联合 Anastrozole、Letrozole 等激素疗法,或mTOR、AKT、PI3K抑制剂,或免疫治疗。
2 靶向 HER2 的激酶抑制剂
与其他生长因子受体类似,HER2的胞内部分(延伸至细胞质的区域)是激酶。当HER2与自身或其他HER家族成员结合后,受体相互磷酸化并激活多种信号通路。由于HER2是激酶,因此可研发靶向它的激酶抑制剂。但在 HER2阳性乳腺癌中,基于抗体的治疗效果更为显著,因此HER2靶向抗体的应用远比激酶抑制剂广泛。
2.1 HER2 靶向激酶抑制剂对比
在欧洲,目前有三种激酶抑制剂获批用于HER2阳性乳腺癌:拉帕替尼、奈拉替尼和图卡替尼(见表2)。拉帕替尼与许多其他激酶抑制剂一样,模拟ATP可逆性阻断EGFR和 HER2 的 ATP 结合位点。与HER2靶向抗体不同,它可阻断持续激活的短链HER2(p95)。
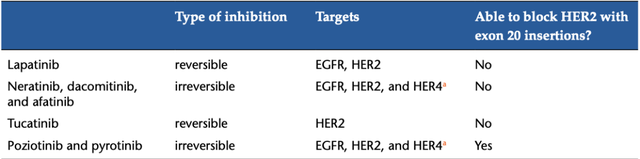
表2 Her2靶向激酶抑制剂的比较
奈拉替尼与阿法替尼、达可替尼一样,是不可逆的泛 HER 抑制剂(可阻断所有 HER 家族成员,而非仅HER2和 EGFR)。2018 年 9 月,欧洲药品管理局(EMA)批准奈拉替尼作为辅助治疗,用于术后完成标准曲妥珠单抗治疗(1 年)的早期HER2阳性乳腺癌患者。
图卡替尼是较新的药物,为高特异性可逆性 HER2 抑制剂,目前获批用于已接受其他HER2靶向治疗的晚期HER2阳性乳腺癌患者,FDA 还批准其用于经治的HER2阳性肠癌患者。
2.2 对脑转移的活性
约 50% 的 HER2 阳性乳腺癌患者会发生脑转移,这主要是因为基于抗体的治疗可清除全身其他部位的癌细胞,使患者生存期延长,从而为脑转移的发生提供了时间。
激酶抑制剂相比抗体类药物的理论优势在于其可能穿过血脑屏障,预防或控制脑转移。多项试验表明,拉帕替尼、奈拉替尼和图卡替尼等激酶抑制剂对已有脑转移或存在转移风险的患者均有获益。但实际情况并非绝对,有明确证据显示部分抗体类药物也可作用于脑转移。例如,DESTINY-Breast03 试验中,T-DXd(抗体偶联药物)对脑转移有显著疗效。
2.3 HER2 外显子 20 插入突变的癌症
HER2 基因扩增是乳腺癌和其他部分癌症中最常见的 HER2 基因突变类型。但在非小细胞肺癌(NSCLC)中,最常见的 HER2 基因突变影响其激酶结构域,这类突变通常发生在外显子 20,与 EGFR 基因外显子 20 插入突变的影响类似。
基于 DESTINY-Lung02 试验,德曲妥珠单抗(T-DXd)于2022年成为首个获批用于治疗HER2突变NSCLC的药物。此外,波奇替尼和吡咯替尼在 HER2 突变 NSCLC 中也显示出积极结果。这些治疗可能也适用于少数由 HER2 外显子 20 插入驱动的其他癌症(如乳腺癌、膀胱癌和中枢神经系统癌症)。
2.4 耐药机制
HER2 靶向激酶抑制剂的耐药原因与抗体类药物类似,例如 HER2 基因突变、存在替代生长因子受体(如 HER3)以及 PI3K/AKT/mTOR 通路突变等,均会导致对 HER2 靶向激酶抑制剂的耐药。

